輝瑞很狂,狂推PF-07321332

(圖片引自網路)
輝瑞一下子就搞兩個試驗,第一個,
輝瑞PF-07321332(片劑) +利托那韋(膠囊),對非住院,高風險之新冠感染成人,進行FDA之2+3期試驗,目前招收個案中,
其ClinicalTrials.gov 標識碼:NCT04960202
該試驗計畫首次發布 : 2021年 7月13日,最後更新發布: 2021年9月1日。
該研究的目的是確定PF-07321332 +利托那韋對於治療患有 COVID-19且不需要住院但患重病風險增加的成年人是否安全有效。總研究時間長達 24 週。
預計招收人數:3000名參與者
試驗設計:隨機、雙盲、實驗組對照組(平行配置)設計,1:1設計
處遇:接受PF-07321332+利托那韋或安慰劑,每 12 小時口服一次,持續5天(共10劑)(沒說明劑量)。
實際試驗開始日期:2021年7月16日
預計主要療效指標完成日期:2021年10月16日
預計研究完成日期:2022年2月26日
主要療效測量 :
因任何原因導致 COVID-19 相關住院或死亡的參與者比例 [時間範圍:第1天至第28天]
次要療效測量 :
PF-07321332/利托那韋相對於安慰劑的不良事件(AE)和嚴重不良事件(SAE)的發生率[時間範圍:第1天至第34天]
PF-07321332/利托那韋相對於安慰劑PF-07321332/利托那韋相對於安慰劑的治療出現的不良事件(TEAE)的發生率[時間範圍:第1天至第34天]
每個目標 COVID-19 跡象/症狀的持續時間 [時間範圍:第1天到第28天]
每個目標 COVID-19 跡象/症狀的嚴重程度 [時間範圍:第1天到第28天]
死亡的參與者比例(全因)[時間範圍:第1天到第24週]
確定PF-07321332血漿和全血中PF-07321332在患有 COVID 19 且進展為嚴重疾病風險增加的非住院有症狀成年參與者中的藥代動力學 (PK) [時間範圍:第1天至第5天]
通過反轉錄聚合酶鏈反應 (RT-PCR) 在鼻拭子中測量病毒滴度 [時間範圍:第 1天到第14天]
除住院外的 COVID-19 相關醫療就診次數 [時間範圍:第1天至第34天]
住院和重症監護室治療 COVID-19 的天數 [時間範圍:第1天至第34天]
第二個試驗,是新開的,還沒招收病人
是研究PF-07321332+利托那韋,對非住院治療,低風險,感染COVID-19成人,
其ClinicalTrials.gov 標識碼:NCT05011513
招聘現狀 : 還沒招人
試驗計畫首次發布 : 2021 年 8 月 18 日
最後更新發布 : 2021 年 8 月 23 日
試驗測試的主要假設是PF-07321332+利托那韋和安慰劑之間在第 28 天持續緩解所有COVID-19 症狀的時間是否存在差異。在整個研究期間,將允許在參與者家中或其他非診所地點(如果有)進行研究訪問。總研究時間長達 24 週。
預計招收人數:1140 名參與者
試驗設計:隨機、雙盲、實驗組對照組(平行配置)設計,1:1設計
處遇:接受 PF-07321332/利托那韋或安慰劑,每 12 小時口服一次,持續5天(共10劑)(沒說明劑量)。
預計學習開始日期 : 2021 年 8 月 19 日
預計主要完成日期 : 2021 年 10 月 18 日
預計研究完成日期 : 2022 年 2 月 28 日
主要結果測量 :
持續緩解所有的 COVID-19症狀的時間 [時間範圍:基線至第28天](分析包括治療前1-3天出現的COVID-19症狀。)
次要結果測量 :
經歷不良事件 (AE) 的參與者百分比 [時間範圍:基線至第34天]
經歷導致研究中止的 AE 或嚴重不良事件 (SAE) 的參與者百分比 [時間範圍:基線至第34天]
因 COVID-19 而出現嚴重體徵/症狀的參與者比例 [時間範圍:基線至第28天]
持續解決所有有針對性的 COVID-19 跡象/症狀的時間 [時間範圍:基線至第28天]
每個目標 COVID-19 徵兆/症狀的持續時間 [時間範圍:基線到第28天]
在 1 個或多個 COVID-19 跡象/症狀中進展到惡化狀態的參與者比例 [時間範圍:基線到第28天]
安靜時外周血氧飽和度 ≥ 95% 的參與者比例 [時間範圍:第 1、5天]
COVID-19 相關醫療就診次數 [時間範圍:基線至第 28天]
COVID-19 相關住院參與者的住院天數和重症監護病房 (ICU) 天數 [時間框架:基線至第28天]
因 COVID-19 相關住院或因任何原因死亡的參與者比例 [時間範圍:基線至第28天]
死亡(全因)參與者的比例 [時間範圍:基線到第 24週]
PF-07321332 的最低濃度(Ctrough)[時間範圍:基線到第 5天]
通過鼻拭子中的逆轉錄聚合酶鏈反應 (RT-PCR) 測量病毒滴度 [時間範圍:基線至第14天]
持續緩解所有有針對性的 COVID-19 症狀的時間 [時間範圍:基線至第28天]
(分析包括治療前 1-5 天出現的 COVID-19症狀。)
~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~
阿土博原以為輝瑞CEO博爾拉(Albert Bourla)

(圖片引自https://money.udn.com/money/story/5658/5419683)
他四月只是嘴砲一下,沒想到是玩真的,還玩這麼大!
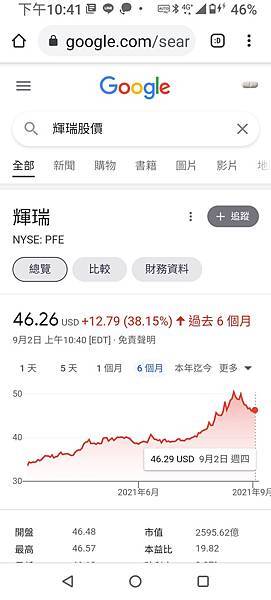
結果輝瑞從七月初40元漲到八月中50元附近,就是部分反映試驗利多消息。
輝瑞一下子要吸走中重症3000人,以後還要吸走輕中症1140人,其他新新股試驗收案,將很辛苦啊,很期待國內新新股二期作完,趕快授權大廠合作三期試驗,以夷制夷!
說真的,大廠有錢就可以任性,隨便開3000人,藥只要有低效果量,就隨便達到顯著,擺明就是要用數量壓死人,要達統計顯著性,笑死人,人海戰術就行!



 留言列表
留言列表


 {{ article.title }}
{{ article.title }}